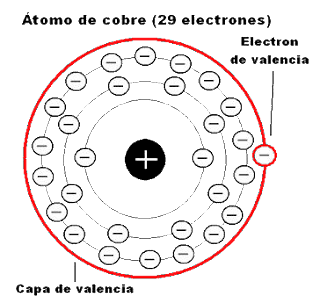
 Ya hemos visto la corteza atómica y la estructura electrónica, ya solo queda ver la capa de valencia.
Ya hemos visto la corteza atómica y la estructura electrónica, ya solo queda ver la capa de valencia.La capa de valencia es la última capa donde se alojan los electrones en la corteza. En el caso del Boro (B), la configuración electrónica es 1s2 2s2 2p1, eso nos indica que su capa de valencia es 2; y los electrones de valencia (nº de electrones que hay en la capa de valencia) es 3.
Para ver esto, es mejor hacerlo por medio de ejercicios así que vamos a realizar uno para que quede claro.
1. Indica la configuración electrónica, la capa de valencia y los electrones de valencia de los siguientes elementos:
- Ne (Z=10) -- 1s2 2s2 2p6 -- Capa de valencia: 2 -- e- de valencia: 8 (6+2)
- N (Z=7) -- 1s2 2s2 2p3 -- Capa de valencia: 2 -- e- de valencia: 5 (3+2)
- Cl (Z=17) -- 1s2 2s2 2p6 3s2 3p5 -- Capa de valencia: 3 -- e- de valencia: 7 (5+2)
Por último vamos a ver como se ordenan los elementos en la tabla periódica. Como sabemos se ordenan por grupos (18) y periodos (7), gracias a ello podemos saber los e- de valencia y la capa de valencia en la siguiente "tabla" siendo "n" el número del periodo:
Grupo 1 -- n s1
Grupo 2 -- n s2
Grupo 13 -- n s2 n p1
Grupo 14 -- n s2 n p2
Grupo 15 -- n s2 n p3
Grupo 16 -- n s2 n p4
Grupo 17 -- n s2 n p5
Grupo 18 -- n s2 n p6
¿por qué se suman los electrones de las dos últimas capas? No se contaría solo el número de la última?
ResponderEliminarEs decir, por qué por ejemplo en este caso, suman? ---->1s2 2s2 2p6 -- Capa de valencia: 2 -- e- de valencia: 8 (6+2) por qué se suman ayudaa por favor
en los numeros cuanticos, los que tu ves allí (1s2 2s2 2p6) el numero de la izquiera, por ejemplo en 1s2 representa el nivel (o capa de valencia), es así que un nivel tiene subniveles, representqados por las letras s, p, d, f respectivamente, para el caso de la segunda capa n=2 hay dos subniveles donde se alojan los electrones (s, p) el numero de la derecha te indica cuántos electrones existen en ese subnivel siendo asi cada subnivel con un numero máximo de electrones s:max 2; p: max 6, d:max10 y f:max 14.....en ese elemento, existen dos niveles, el primer nivel (1) tiene un subnivel (s) con dos electrones (2) y el segundo nivel (2) tiene dos subniveles: s con 2 electrones, y p con 6 electrones, teniendo como resultado para la capa de valencia (2) un total de 8 electrones localizados en diferentes SUB niveles pertenecientes a esta capa.
EliminarEspero que te haya sido útil.
Saludos.
Verás, te lo pondré con un ejemplo: En 1s2 2s2 2p6, la capa de Valencia está claro que es dos. Los electrones de Valencia es el número de electrones que hay en la capa de Valencia, por tanto en la 2. En este caso hay 2 y 6 electrones de Valencia por tanto es 8. Lo ves ahora más claro? Si no, mándame un correo a fisicayquimicasegundocicloeso.blogspot.com y te atenderé en seguida con un dibujo para que lo termines de ver.
Eliminaren los numeros cuanticos, los que tu ves allí (1s2 2s2 2p6) el numero de la izquiera, por ejemplo en 1s2 representa el nivel (o capa de valencia), es así que un nivel tiene subniveles, representqados por las letras s, p, d, f respectivamente, para el caso de la segunda capa n=2 hay dos subniveles donde se alojan los electrones (s, p) el numero de la derecha te indica cuántos electrones existen en ese subnivel siendo asi cada subnivel con un numero máximo de electrones s:max 2; p: max 6, d:max10 y f:max 14.....en ese elemento, existen dos niveles, el primer nivel (1) tiene un subnivel (s) con dos electrones (2) y el segundo nivel (2) tiene dos subniveles: s con 2 electrones, y p con 6 electrones, teniendo como resultado para la capa de valencia (2) un total de 8 electrones localizados en diferentes SUB niveles pertenecientes a esta capa.
ResponderEliminarEspero que te haya sido útil.
Saludos.
Como puedo saber cuál es la capa de valencia de ,por ejemplo, Br?
ResponderEliminarDebes mirarlo en la tabla periódica. Tienes 2 opciones: 1) Mirar su Z y hacer su configuración electrónica ò 2) Ver en que periodo está de la tabla periódica.
EliminarCapa de valencia del bromo : 4. Electrones de valencia : 7.
Configuración electrónica Br : 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4s5
... 3d10 4p5
Eliminar1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5 esta es la configuraciòn del bromo que me sale
ResponderEliminar¡PERFECTO! un 10
EliminarMadre mia... La seño lo explicó como si fuera que te convalidaran la NASA, pero leo aquí y resulta que es facilísimo. Ya no podré trabajar allí pero la nota si que va a ser buena.
ResponderEliminarGracias!
¡De nada!
Eliminarla capa de valencia siempre será la más externa?
ResponderEliminarla capa de valencia siempre será la más externa?
ResponderEliminarSí, se define así. Muchas gracias.
Eliminarmolibdeno? capa de valencia?
ResponderEliminartiene configuracion electronica inestable
Pero si tu tienes dos capas como 4s2 y luego 3d5 la capa de valencia cual es? Porque a capa 4 y la tres no están acabadas.
ResponderEliminarYa, pero siguiendo la definición, es la 4, porque la capa 4 es la más externa. La 3d es una capa que está más interna. Muchas gracias.
EliminarQuisiera saber por que para el hierro para hallar su electron de valencia se utiliza la capa mas externa y la energetica? Necesito ayuda por favorrr!!
ResponderEliminar¿Que sucede si la capa de Valencia esta extendida?
ResponderEliminary como se sabe el periodo????
ResponderEliminarCapa de Valencia para el Níquel? No es 4?
ResponderEliminarEsto es fabuloso
ResponderEliminarhola chupame las bolas
ResponderEliminarperdon por la mala palabra, me sirvio mucho esta informacion
Eliminarpedazo de puto
ResponderEliminarHijoooo deeeee laaaaa perraaaaaaa
ResponderEliminarEstan de la capa de invisibilidad
ResponderEliminarNecesito Ayuda, Necesito Encontrar La Capa De Valencia De 1s2 2s2 2p6 3s1, Como Lo Hago?
ResponderEliminarla capa de valencia es 3 y los electrones es 4
Eliminar3s1, tiene un electron
ResponderEliminarNecesito ayuda con la regla de Octeto
ResponderEliminarRelacion entre capa de valencia y Electrones de valencia Porfavor
ResponderEliminarNo entiendo nada, ayudaaa
ResponderEliminarse tiene 4 atomos neutros de los elementos abcyd
ResponderEliminara tiene 6 electrones en su capa de valencia
b tiene 5 electrones en su capa de valencia
c tiene 4 electrones en su capa de valencia
d tiene7 electrones en su capa de valencia
ay b tiene menos 10 electrones
cyd tienen entre 13 y 18 electrones
indique la ideantidad de lo elementos en cuestin
Cuantos electrones de valencia tiene este elemento:1s2 2s2 2p6 y porque
ResponderEliminarnecesito encontrar la capa de valencias de hidrogeno, fosforo, cobre y zink
ResponderEliminarpor favor
Nunca he sido de ir a la peluquería cuando he tenido una fiesta o boda importante. Yo misma me arreglaba el pelo y arreando, no me daba el sueldo para más. Pero un día, hará unos cuatro años, invitada a una boda en la que quería estar cañón, se me ocurrió acabar con la costumbre la-voz.net/la-estela-raimondi/
ResponderEliminarUna pregunta, no se mucho del tema, la capa de valencia es la capa electrónica más externa como se ve en el dibujo, o es el orbital más externo?
ResponderEliminarhola buenas tardes
ResponderEliminar